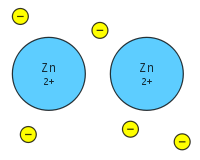
Ένας μεταλλικός δεσμός είναι ο διαμοιρασμός πολλών αποσπασμένων ηλεκτρονίων μεταξύ πολλών θετικών ιόντων, όπου τα ηλεκτρόνια δρουν ως "κόλλα" δίνοντας στην ουσία μια συγκεκριμένη δομή. Διαφέρει από τον ομοιοπολικό ή τον ιοντικό δεσμό. Τα μέταλλα έχουν χαμηλή ενέργεια ιονισμού. Ως εκ τούτου, τα ηλεκτρόνια σθένους μπορούν να αποδιαταχθούν σε όλα τα μέταλλα. Τα αποεντοπισμένα ηλεκτρόνια δεν συνδέονται με έναν συγκεκριμένο πυρήνα ενός μετάλλου, αλλά είναι ελεύθερα να κινούνται σε ολόκληρη την κρυσταλλική δομή σχηματίζοντας μια "θάλασσα" ηλεκτρονίων.
Τα ηλεκτρόνια και τα θετικά ιόντα στο μέταλλο έχουν ισχυρή ελκτική δύναμη μεταξύ τους. Ως εκ τούτου, τα μέταλλα έχουν συχνά υψηλά σημεία τήξης ή βρασμού. Η αρχή είναι παρόμοια με εκείνη των ιοντικών δεσμών.
Οι μεταλλικοί δεσμοί προκαλούν πολλά από τα χαρακτηριστικά των μετάλλων, όπως αντοχή, πλαστιμότητα, ολκιμότητα, λάμψη, αγωγιμότητα της θερμότητας και του ηλεκτρισμού.
Επειδή τα ηλεκτρόνια κινούνται ελεύθερα, το μέταλλο έχει κάποια ηλεκτρική αγωγιμότητα. Αυτό επιτρέπει στην ενέργεια να περάσει γρήγορα μέσα από τα ηλεκτρόνια, δημιουργώντας ηλεκτρικό ρεύμα. Τα μέταλλα αγωγιμοποιούν τη θερμότητα για τον ίδιο λόγο: τα ελεύθερα ηλεκτρόνια μπορούν να μεταφέρουν την ενέργεια με γρηγορότερο ρυθμό από ό,τι άλλες ουσίες με ηλεκτρόνια που είναι στερεωμένα στη θέση τους. Υπάρχουν επίσης λίγα μη μέταλλα που αγωγιμοποιούν τον ηλεκτρισμό: ο γραφίτης (επειδή, όπως και τα μέταλλα, έχει ελεύθερα ηλεκτρόνια) και οι ιοντικές ενώσεις που είναι λιωμένες ή διαλυμένες στο νερό, οι οποίες έχουν ελεύθερα κινούμενα ιόντα.
Οι μεταλλικοί δεσμοί έχουν τουλάχιστον ένα ηλεκτρόνιο σθένους το οποίο δεν μοιράζονται με γειτονικά άτομα και δεν χάνουν ηλεκτρόνια για να σχηματίσουν ιόντα. Αντίθετα, οι εξωτερικές ενεργειακές στάθμες (ατομικά τροχιακά) των ατόμων του μετάλλου επικαλύπτονται. Είναι παρόμοιοι με τους ομοιοπολικούς δεσμούς. Δεν παρουσιάζουν όλα τα μέταλλα μεταλλικό δεσμό. Για παράδειγμα, τα ιόντα υδραργύρου (Hg2+
2) σχηματίζουν ομοιοπολικούς δεσμούς μετάλλου-μετάλλου.
Ένα κράμα είναι ένα διάλυμα μετάλλων. Τα περισσότερα κράματα είναι γυαλιστερά όπως τα καθαρά μέταλλα.