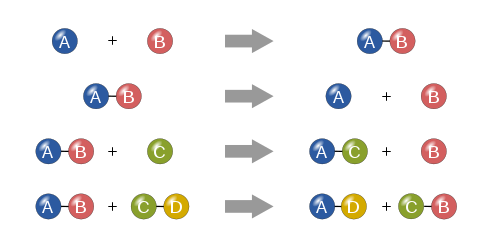
Σύνθεση
Σε μια αντίδραση σύνθεσης, δύο ή περισσότερες απλές ουσίες συνδυάζονται για να σχηματίσουν μια πιο σύνθετη ουσία.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB} 
"Δύο ή περισσότερα αντιδρώντα δίνουν ένα προϊόν" είναι ένας άλλος τρόπος για να προσδιορίσετε μια αντίδραση σύνθεσης. Ένα παράδειγμα αντίδρασης σύνθεσης είναι ο συνδυασμός σιδήρου και θείου προς σχηματισμό σουλφιδίου του σιδήρου(ΙΙ):
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS} 
Ένα άλλο παράδειγμα είναι το απλό αέριο υδρογόνο σε συνδυασμό με απλό αέριο οξυγόνο για την παραγωγή μιας πιο σύνθετης ουσίας, όπως το νερό.
Αποσύνθεση
Μια αντίδραση αποσύνθεσης είναι όταν μια πιο σύνθετη ουσία διασπάται στα πιο απλά μέρη της. Είναι επομένως το αντίθετο της αντίδρασης σύνθεσης και μπορεί να γραφτεί ως εξής:
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B} 
Ένα παράδειγμα αντίδρασης διάσπασης είναι η ηλεκτρόλυση του νερού για την παραγωγή αερίου οξυγόνου και υδρογόνου:
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}} 
Ενιαία αντικατάσταση
Σε μια αντίδραση απλής αντικατάστασης, ένα μόνο μη συνδυασμένο στοιχείο αντικαθιστά ένα άλλο σε μια ένωση- με άλλα λόγια, ένα στοιχείο ανταλλάσσει θέσεις με ένα άλλο στοιχείο σε μια ένωση:
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} 
Ένα παράδειγμα αντίδρασης απλής μετατόπισης είναι όταν το μαγνήσιο αντικαθιστά το υδρογόνο στο νερό για να παραχθεί υδροξείδιο του μαγνησίου και αέριο υδρογόνο:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}}} 
Διπλή αντικατάσταση
Σε μια αντίδραση διπλής αντικατάστασης, τα ανιόντα και τα κατιόντα δύο ενώσεων αλλάζουν θέσεις και σχηματίζουν δύο εντελώς διαφορετικές ενώσεις. Οι αντιδράσεις αυτές έχουν τη γενική μορφή:
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB} 
Για παράδειγμα, όταν αντιδρούν το χλωριούχο βάριο (BaCl2 ) και το θειικό μαγνήσιο (MgSO4 ), το 42−ανιόν SO αλλάζει θέση με το ανιόν 2Cl−, δίνοντας τις ενώσεις BaSO4και MgCl 2.
Ένα άλλο παράδειγμα αντίδρασης διπλής μετατόπισης είναι η αντίδραση του νιτρικού μολύβδου(ΙΙ) με ιωδιούχο κάλιο προς σχηματισμό ιωδιούχου μολύβδου(ΙΙ) και νιτρικού καλίου:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}}