Το μοντέλο της πουτίγκας δαμάσκηνου ήταν ένα πρώιμο (και λανθασμένο) μοντέλο του 20ού αιώνα για το άτομο. Προτάθηκε από τον J.J. Thomson το 1904, μετά την ανακάλυψη του ηλεκτρονίου, αλλά πριν από την ανακάλυψη του ατομικού πυρήνα. Εκείνη την εποχή, οι επιστήμονες γνώριζαν ότι υπήρχε ένα θετικό φορτίο στο άτομο που εξισορροπούσε τα αρνητικά φορτία των ηλεκτρονίων, καθιστώντας το άτομο ουδέτερο, αλλά δεν γνώριζαν από πού προερχόταν το θετικό φορτίο. Το μοντέλο του Thomson έδειχνε ένα άτομο που είχε ένα θετικά φορτισμένο μέσο, ή χώρο, με αρνητικά φορτισμένα ηλεκτρόνια μέσα στο μέσο. Σύντομα μετά την πρότασή του, το μοντέλο ονομάστηκε μοντέλο "πουτίγκα δαμάσκηνου", επειδή το θετικό μέσο ήταν σαν πουτίγκα, με ηλεκτρόνια ή δαμάσκηνα στο εσωτερικό της.
Ατομικό μοντέλο του σταφιδόψωμου
Ανάπτυξη στο σύγχρονο ατομικό μοντέλο
Το μοντέλο του Rutherford
Βασικά, το 1909, λίγο καιρό μετά την πρόταση του μοντέλου του Thomson, ο Hans Geiger και ο Ernest Marsden έκαναν ένα πείραμα με λεπτά φύλλα χρυσού, για να ελέγξουν το μοντέλο του Thomson. Ο καθηγητής τους, Ernest Rutherford, περίμενε ότι τα αποτελέσματα θα αποδείκνυαν ότι ο Thomson είχε δίκιο, αλλά τα αποτελέσματά τους ήταν εξαιρετικά διαφορετικά από αυτά που περίμεναν. Το 1911, ο Ράδερφορντ ανακάλυψε ότι τα θετικά φορτία προέρχονται από μικροσκοπικά σωματίδια που ονομάζονται πρωτόνια και ότι τα πρωτόνια βρίσκονταν σε ένα μικροσκοπικό κέντρο που ονομάζεται πυρήνας και ότι τα ηλεκτρόνια περιφέρονταν γύρω από τον πυρήνα.
Μοντέλο Bohr
Το μοντέλο του Ράδερφορντ ήταν αρκετά απλό, αλλά ήταν λανθασμένο, διότι τα ηλεκτρόνια έχουν φορτίο και θα έπρεπε να έλκονται από τον θετικά φορτισμένο πυρήνα. Το 1913, ο Niels Bohr πρόσθεσε στο ατομικό μοντέλο τα "ενεργειακά επίπεδα". Τα ηλεκτρόνια δεν πέφτουν στον πυρήνα επειδή περιέχονται σε ενεργειακά επίπεδα, και για να μεταβούν σε υψηλότερα ενεργειακά επίπεδα απαιτείται επιπλέον ενέργεια, ενώ για να μεταβούν σε χαμηλότερα ενεργειακά επίπεδα απαιτείται απελευθέρωση ενέργειας. Δεν είναι δυνατόν να αλλάξουμε ενεργειακές καταστάσεις χωρίς να αλλάξουμε την ενέργεια του ηλεκτρονίου. Αν ένα ηλεκτρόνιο χτυπηθεί από ένα φωτόνιο (σωματίδιο που μεταφέρει ηλεκτρομαγνητική ακτινοβολία), θα αποκτήσει επιπλέον ενέργεια και θα μεταβεί σε υψηλότερη ενεργειακή στάθμη (αλλάζει κατάσταση), και στη συνέχεια θα μεταπηδήσει ξανά σε χαμηλότερη ενεργειακή στάθμη, απελευθερώνοντας την ενέργεια που περιέχει. Αυτό το νέο μοντέλο ονομάστηκε μοντέλο Bohr ή μοντέλο Rutherford-Bohr. Αυτό προσέθεσε έναν εντελώς νέο κλάδο της επιστήμης: Κβαντική φυσική.
Κβαντικό μοντέλο
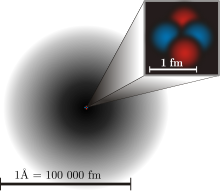
Το 1926 ο Έρβιν Σρέντινγκερ χρησιμοποίησε την ιδέα ότι τα ηλεκτρόνια δρουν ως κύματα και ως σωματίδια, κάτι που είναι γνωστό ως δυϊσμός κύματος-σωματιδίου. Αυτό πρόσθεσε ένα εντελώς νέο επίπεδο στο ατομικό μοντέλο και στην κβαντική φυσική. Με ένα σωματίδιο, μπορείτε να ξέρετε πού βρίσκεται στο χώρο αν το παρατηρήσετε (κοιτάξετε). Αλλά με ένα κύμα, βρίσκεται παντού, οπότε δεν μπορείτε να προσδιορίσετε πού ακριβώς βρίσκεται. Αυτό είναι γνωστό ως κβαντική αβεβαιότητα. Με ένα ηλεκτρόνιο, μπορείτε να γνωρίζετε μόνο την πιθανότητα να βρίσκεται σε ένα μέρος, επειδή είναι κύμα καθώς και σωματίδιο. (Βλέπε παραπάνω διάγραμμα)


Σχετικές σελίδες
- Ατομική θεωρία
- Κβαντομηχανική
- J. J. Thomson
- Ernest Rutherford
- Niels Bohr
- Erwin Schrödinger
