Η αντίδραση SN 2 (επίσης γνωστή ως διμοριακή πυρηνόφιλη υποκατάσταση) είναι μια αντίδραση υποκατάστασης στην οργανική χημεία. Είναι ένας τύπος πυρηνόφιλης υποκατάστασης, όπου ένα μοναχικό ζεύγος από ένα πυρηνόφιλο επιτίθεται σε ένα ηλεκτρόφιλο κέντρο με έλλειψη ηλεκτρονίων και συνδέεται με αυτό. Αυτό αποβάλλει μια άλλη ομάδα που ονομάζεται "αποχωρούσα ομάδα". Έτσι, η εισερχόμενη ομάδα αντικαθιστά την αποχωρούσα ομάδα σε ένα βήμα. Δεδομένου ότι δύο αντιδρώντα είδη εμπλέκονται στο αργό, καθοριστικό για την ταχύτητα βήμα της αντίδρασης, αυτό οδηγεί στην ονομασία διμοριακή πυρηνόφιλη υποκατάσταση ή SN 2. Μεταξύ των ανόργανων χημικών, η αντίδραση SN 2 είναι συχνά γνωστή ως μηχανισμός ανταλλαγής.
SN2 αντίδραση
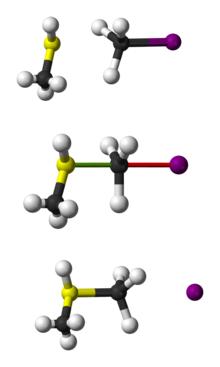

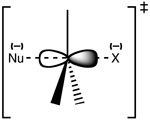

Μηχανισμός αντίδρασης
Η αντίδραση συμβαίνει συχνότερα σε ένα αλειφατικό sp3 κέντρο άνθρακα με μια ηλεκτροαρνητική, σταθερή αποχωρούσα ομάδα συνδεδεμένη με αυτό - "Χ" - συχνά ένα άτομο αλογονιδίου. Η διάσπαση του δεσμού C-X και ο σχηματισμός του νέου δεσμού C-Nu συμβαίνουν ταυτόχρονα για να σχηματιστεί μια μεταβατική κατάσταση στην οποία ο άνθρακας που δέχεται πυρηνόφιλη επίθεση είναι πεντασυντεταγμένος και περίπου sp2 υβριδισμένος. Το πυρηνόφιλο επιτίθεται στον άνθρακα σε γωνία 180° ως προς την αποχωρούσα ομάδα, καθώς αυτό παρέχει την καλύτερη επικάλυψη μεταξύ του μοναχικού ζεύγους του πυρηνόφιλου και του αντιδεσμικού τροχιακού C-X σ*. Στη συνέχεια, η αποχωρούσα ομάδα ωθείται από την αντίθετη πλευρά και σχηματίζεται το προϊόν.
Εάν το υπόστρωμα που δέχεται πυρηνόφιλη επίθεση είναι χειρόμορφο, αυτό μπορεί να οδηγήσει, αν και όχι απαραίτητα, σε αναστροφή της στερεοχημείας, που ονομάζεται αναστροφή Walden.
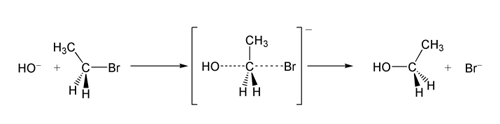
Σε ένα παράδειγμα της αντίδρασης SN 2, η επίθεση του ΟΗ −(το πυρηνόφιλο) σε ένα βρωμοαιθάνιο (το ηλεκτρόφιλο) οδηγεί σε αιθανόλη, με το βρωμίδιο να εκτινάσσεται ως αποχωρούσα ομάδα:
Μια αντίδραση SN 2 λαμβάνει χώρα εάν η οπισθόδρομος προσβολής δεν εμποδίζεται από άλλα άτομα του μορίου (στερικά παρεμποδίζεται από υποκαταστάτες στο υπόστρωμα). Έτσι, αυτός ο μηχανισμός εμφανίζεται συνήθως σε ένα ανεμπόδιστο πρωτογενές κέντρο άνθρακα. Εάν υπάρχει στερικός συνωστισμός στο υπόστρωμα κοντά στην αποχωρούσα ομάδα, όπως σε ένα τριτοταγές κέντρο άνθρακα, η υποκατάσταση θα χρησιμοποιήσει έναν μηχανισμό SN 1 παρά έναν μηχανισμό SN 2, (ένας μηχανισμός SN 1 θα ήταν επίσης πιο πιθανός με μπλοκαρισμένα μόρια, επειδή θα μπορούσε να σχηματιστεί ένα επαρκώς σταθερό ενδιάμεσο καρβοκατιόν).
Στη χημεία συντονισμού, η συνειρμική υποκατάσταση πραγματοποιείται με παρόμοιο μηχανισμό όπως το SN 2.
Παράγοντες που επηρεάζουν την ταχύτητα της αντίδρασης
Τέσσερις παράγοντες επηρεάζουν την ταχύτητα της αντίδρασης:
- Υπόστρωμα. Το υπόστρωμα παίζει τον σημαντικότερο ρόλο στον καθορισμό του ρυθμού της αντίδρασης. Αυτό οφείλεται στο γεγονός ότι το πυρηνόφιλο επιτίθεται από το πίσω μέρος του υποστρώματος, σπάζοντας έτσι τον δεσμό της ομάδας που αφήνει άνθρακα και σχηματίζοντας τον δεσμό άνθρακα-πυρηνόφιλο. Επομένως, για να μεγιστοποιηθεί ο ρυθμός της αντίδρασης SN 2, το πίσω μέρος του υποστρώματος πρέπει να είναι όσο το δυνατόν πιο ανεμπόδιστο. Συνολικά, αυτό σημαίνει ότι τα μεθυλικά και τα πρωτογενή υποστρώματα αντιδρούν ταχύτερα, ακολουθούμενα από τα δευτερογενή υποστρώματα. Τα τριτοταγή υποστρώματα δεν συμμετέχουν στις αντιδράσεις SN 2, λόγω στερικών εμποδίων.
- Πυρηνόφιλο. Όπως και το υπόστρωμα, η στερική παρεμπόδιση επηρεάζει τη δύναμη του πυρηνόφιλου. Το ανιόν του μεθοξειδίου, για παράδειγμα, είναι ταυτόχρονα ισχυρή βάση και πυρηνόφιλο, επειδή είναι πυρηνόφιλο του μεθυλίου, και επομένως είναι πολύ ανεμπόδιστο. Από την άλλη πλευρά, το τερτοβουτοξείδιο είναι ισχυρή βάση, αλλά φτωχό πυρηνόφιλο, επειδή οι τρεις μεθυλομάδες του εμποδίζουν την προσέγγισή του στον άνθρακα. Η δύναμη του πυρηνόφιλου επηρεάζεται επίσης από το φορτίο και την ηλεκτραρνητικότητα: η πυρηνόφιλη δύναμη αυξάνεται με την αύξηση του αρνητικού φορτίου και τη μείωση της ηλεκτραρνητικότητας. Για παράδειγμα, το OH- είναι καλύτερο πυρηνόφιλο από το νερό και το I- είναι καλύτερο πυρηνόφιλο από το Br- (σε πολικούς πρωτικούς διαλύτες). Σε έναν πολικό απρωτικό διαλύτη, η πυρηνόφιλη ιδιότητα αυξάνεται κατά μία στήλη του περιοδικού πίνακα, καθώς δεν υπάρχει δεσμός υδρογόνου μεταξύ του διαλύτη και του πυρηνόφιλου. Στην περίπτωση αυτή, η πυρηνόφιλη αντανακλά τη βασικότητα. Συνεπώς, το I- θα ήταν ασθενέστερο πυρηνόφιλο από το Br- επειδή είναι ασθενέστερη βάση.
- Διαλύτης. Ο διαλύτης επηρεάζει τον ρυθμό της αντίδρασης, επειδή οι διαλύτες μπορεί να περιβάλλουν ή να μην περιβάλλουν ένα πυρηνόφιλο, εμποδίζοντας ή μη την προσέγγισή του στο άτομο άνθρακα. Οι πολικοί απρωτικοί διαλύτες, όπως το τετραϋδροφουράνιο, είναι καλύτεροι διαλύτες για την αντίδραση αυτή από τους πολικούς πρωτικούς διαλύτες, διότι οι πολικοί πρωτικοί διαλύτες θα διαλυθούν από τον υδρογονικό δεσμό του διαλύτη με το πυρηνόφιλο. Αυτό το εμποδίζει να επιτεθεί στον άνθρακα με την αποχωρούσα ομάδα.
- Φεύγοντας από την ομάδα. Η αποχωρούσα ομάδα επηρεάζει την ταχύτητα της αντίδρασης. Όσο πιο σταθερή είναι η αποχωρούσα ομάδα, τόσο πιο πιθανό είναι να πάρει μαζί της τα δύο ηλεκτρόνια της αποχωρούσας ομάδας άνθρακα, όταν το πυρηνόφιλο επιτεθεί στον άνθρακα. Επομένως, όσο ασθενέστερη είναι η αποχωρούσα ομάδα ως συζυγής βάση, τόσο καλύτερη είναι η αποχωρούσα ομάδα. Ομοίως, όσο ισχυρότερο είναι το αντίστοιχο οξύ της, τόσο καλύτερη είναι η αποχωρούσα ομάδα. Παραδείγματα καλών αποχωρητικών ομάδων είναι τα αλογονίδια (εκτός από το φθόριο) και το τοσιλικό. Όμως οι ομάδες HO- και H2 N- δεν είναι καλές αποχωρούσες ομάδες.
Κινητική της αντίδρασης
Ο ρυθμός μιας αντίδρασης SN 2 είναι δεύτερης τάξης, καθώς το καθοριστικό για τον ρυθμό βήμα εξαρτάται από τη συγκέντρωση του πυρηνόφιλου, [Nu− ], καθώς και από τη συγκέντρωση του υποστρώματος, [RX].
r = k[RX][Nu− ]
Αυτή είναι μια βασική διαφορά μεταξύ των μηχανισμών SN 1 και SN 2. Στην αντίδραση SN 1, το νουκλεόφιλο επιτίθεται μετά το τέλος του περιοριστικού βήματος. Στην αντίδραση SN 2, όμως, το πυρηνόφιλο απομακρύνει την αποχωρούσα ομάδα στο περιοριστικό βήμα. Με άλλα λόγια, ο ρυθμός των αντιδράσεων SN 1 εξαρτάται μόνο από τη συγκέντρωση του υποστρώματος, ενώ ο ρυθμός της αντίδρασης SN 2 εξαρτάται από τη συγκέντρωση τόσο του υποστρώματος όσο και του πυρηνόφιλου. Σε περιπτώσεις όπου είναι δυνατοί και οι δύο μηχανισμοί (για παράδειγμα σε ένα δευτερογενές κέντρο άνθρακα), ο μηχανισμός εξαρτάται από τον διαλύτη, τη θερμοκρασία, τη συγκέντρωση του πυρηνόφιλου ή από την αποχωρούσα ομάδα.
Οι αντιδράσεις SN 2 ευνοούνται γενικά σε πρωτογενή αλκυλαλογονίδια ή δευτερογενή αλκυλαλογονίδια με απρωτικό διαλύτη. Εμφανίζονται με αμελητέο ρυθμό σε τριτοταγή αλκυλαλογονίδια λόγω στερικών εμποδίων.
SN 2 και SN 1 είναι τα δύο άκρα μιας ολισθαίνουσας κλίμακας αντιδράσεων. Είναι δυνατόν να βρεθούν πολλές αντιδράσεις που παρουσιάζουν στους μηχανισμούς τους τόσο τον χαρακτήρα SN 2 όσο και SN 1. Για παράδειγμα, είναι δυνατόν να προκύψουν ζεύγη ιόντων επαφής που σχηματίζονται από ένα αλκυλαλογονίδιο στα οποία τα ιόντα δεν διαχωρίζονται πλήρως. Όταν αυτά υποστούν υποκατάσταση, η στερεοχημεία θα αντιστραφεί (όπως στο SN 2) για πολλά από τα αντιδρώντα μόρια, αλλά μερικά μπορεί να παρουσιάσουν διατήρηση της διαμόρφωσης. Οι αντιδράσεις SN 2 είναι πιο συχνές από τις αντιδράσεις SN 1.
Ανταγωνισμός E2
Μια συνήθης δευτερεύουσα αντίδραση που λαμβάνει χώρα με τις αντιδράσεις SN 2 είναι η απαλοιφή E2: το εισερχόμενο ανιόν μπορεί να δράσει ως βάση και όχι ως πυρηνόφιλο, αφαιρώντας ένα πρωτόνιο και οδηγώντας στο σχηματισμό του αλκενίου. Το φαινόμενο αυτό μπορεί να καταδειχθεί στην αντίδραση σε αέρια φάση μεταξύ ενός σουλφονικού άλατος και ενός απλού βρωμιούχου αλκυλίου που λαμβάνει χώρα μέσα σε ένα φασματόμετρο μάζας:
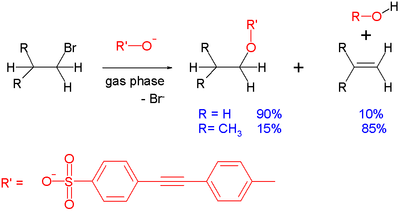
Με το βρωμιούχο αιθύλιο, το προϊόν της αντίδρασης είναι κυρίως το προϊόν υποκατάστασης. Καθώς η στερική παρεμπόδιση γύρω από το ηλεκτροφιλικό κέντρο αυξάνεται, όπως με το βρωμιούχο ισοβουτύλιο, η υποκατάσταση δεν ευνοείται και η εξάλειψη είναι η επικρατούσα αντίδραση. Άλλοι παράγοντες που ευνοούν την εξάλειψη είναι η ισχύς της βάσης. Με το λιγότερο βασικό βενζοϊκό υπόστρωμα, το βρωμιούχο ισοπροπυλο αντιδρά με 55% υποκατάσταση. Γενικά, οι αντιδράσεις φάσης αερίου και οι αντιδράσεις φάσης διαλύματος αυτού του τύπου ακολουθούν τις ίδιες τάσεις, αν και στην πρώτη, οι επιδράσεις του διαλύτη εγκαταλείπονται.
Μηχανισμός κυκλικού κόμβου
Μια εξέλιξη που προσέλκυσε την προσοχή το 2008 αφορά έναν μηχανισμό κυκλικής κίνησης SN 2 που παρατηρήθηκε σε μια αντίδραση σε αέρια φάση μεταξύ ιόντων χλωρίου και ιωδιούχου μεθυλίου με μια ειδική τεχνική που ονομάζεται απεικόνιση με διασταυρωμένη μοριακή δέσμη. Όταν τα ιόντα χλωρίου έχουν επαρκή ταχύτητα, η ενέργεια των ιόντων ιωδίου που προκύπτουν μετά τη σύγκρουση είναι πολύ χαμηλότερη από την αναμενόμενη, και διατυπώνεται η θεωρία ότι η ενέργεια χάνεται ως αποτέλεσμα ενός πλήρους κυκλικού κύκλου της μεθυλομάδας γύρω από το άτομο του ιωδίου πριν λάβει χώρα η πραγματική μετατόπιση.
Σχετικές σελίδες
- Αντίδραση υποκατάστασης
- SN 1 αντίδραση
Ερωτήσεις και απαντήσεις
Ερ: Τι είναι η αντίδραση SN2;
A: Η αντίδραση SN2 είναι μια αντίδραση υποκατάστασης στην οργανική χημεία, όπου ένα πυρηνόφιλο επιτίθεται σε ένα ηλεκτρόφιλο κέντρο με έλλειψη ηλεκτρονίων, αποβάλλοντας μια αποχωρούσα ομάδα και στη συνέχεια αντικαθιστώντας την σε ένα βήμα.
Ερ: Τι είδους αντίδραση υποκατάστασης είναι η αντίδραση SN2;
Α: Η αντίδραση SN2 είναι ένα είδος αντίδρασης πυρηνόφιλης υποκατάστασης.
Ερ: Πόσα αντιδρώντα είδη εμπλέκονται στο αργό, καθοριστικό για την ταχύτητα βήμα της αντίδρασης SN2;
A: Δύο αντιδρώντα είδη συμμετέχουν στο αργό, καθοριστικό για την ταχύτητα βήμα της αντίδρασης SN2.
Ερ: Τι σημαίνει η ονομασία "διμοριακή πυρηνόφιλη υποκατάσταση" για την αντίδραση SN2;
Α: Η ονομασία "διμοριακή πυρηνόφιλη υποκατάσταση" για την αντίδραση SN2 αναφέρεται στο γεγονός ότι δύο αντιδρώντα είδη συμμετέχουν στο αργό, καθοριστικό για την ταχύτητα βήμα της αντίδρασης.
Ερ: Τι είναι το πυρηνόφιλο στο πλαίσιο της αντίδρασης SN2;
A: Πυρηνόφιλο είναι ένα μόριο ή ιόν που δίνει ένα μοναχικό ζεύγος ηλεκτρονίων για να σχηματίσει έναν χημικό δεσμό.
Ερ: Τι είναι το ηλεκτρόφιλο στο πλαίσιο της αντίδρασης SN2;
A: Ηλεκτροφιλικό είναι ένα μόριο ή ιόν που δέχεται ένα ζεύγος ηλεκτρονίων για να σχηματίσει χημικό δεσμό.
Ερ: Πώς είναι συχνά γνωστή η αντίδραση SN2 μεταξύ των ανόργανων χημικών;
Α: Μεταξύ των ανόργανων χημικών, η αντίδραση SN2 είναι συχνά γνωστή ως μηχανισμός ανταλλαγής.