Περιοδικός πίνακας των χημικών στοιχείων
Ο περιοδικός πίνακας των χημικών στοιχείων είναι ένας κατάλογος των γνωστών χημικών στοιχείων. Στον πίνακα, τα στοιχεία τοποθετούνται με τη σειρά των ατομικών τους αριθμών ξεκινώντας από τον μικρότερο αριθμό του ενός, το υδρογόνο. Ο ατομικός αριθμός ενός στοιχείου ταυτίζεται με τον αριθμό των πρωτονίων στον συγκεκριμένο πυρήνα ενός ατόμου. Στον περιοδικό πίνακα τα στοιχεία διατάσσονται σε περιόδους και ομάδες. Μια σειρά στοιχείων στον πίνακα ονομάζεται περίοδος. Κάθε περίοδος έχει έναν αριθμό- από το 1 έως το 8. Η περίοδος 1 έχει μόνο 2 στοιχεία: υδρογόνο και ήλιο. Η περίοδος 2 και η περίοδος 3 έχουν και οι δύο 8 στοιχεία. Άλλες περίοδοι είναι μεγαλύτερες. Τα στοιχεία μιας περιόδου έχουν διαδοχικούς ατομικούς αριθμούς.
Μια στήλη στοιχείων στον πίνακα ονομάζεται ομάδα. Ο τυπικός περιοδικός πίνακας περιλαμβάνει 18 ομάδες. Κάθε ομάδα έχει έναν αριθμό: από το 1 έως το 18. Τα στοιχεία μιας ομάδας έχουν ηλεκτρόνια τοποθετημένα με παρόμοιο τρόπο, ανάλογα με τον αριθμό των ηλεκτρονίων σθένους, γεγονός που τους προσδίδει παρόμοιες χημικές ιδιότητες (συμπεριφέρονται με παρόμοιο τρόπο). Για παράδειγμα, η ομάδα 18 είναι γνωστή ως ευγενή αέρια, επειδή είναι όλα αέρια και δεν συνδυάζονται με άλλα άτομα.
Υπάρχουν δύο συστήματα ομαδικών αριθμών: το ένα χρησιμοποιεί αραβικούς αριθμούς (1,2,3) και το άλλο λατινικούς αριθμούς (I, II, III). Οι λατινικοί αριθμοί χρησιμοποιήθηκαν στο μεγαλύτερο μέρος του 20ού αιώνα. Το 1990 η Διεθνής Ένωση Καθαρής και Εφαρμοσμένης Χημείας (IUPAC) αποφάσισε να χρησιμοποιήσει το νέο σύστημα με αραβικούς αριθμούς, για να αντικαταστήσει τα δύο παλαιά συστήματα ομάδων που χρησιμοποιούσαν λατινικούς αριθμούς.
Ο περιοδικός πίνακας χρησιμοποιήθηκε από τους χημικούς για να παρατηρήσουν τα πρότυπα και τις σχέσεις μεταξύ των στοιχείων. Ο Περιοδικός Πίνακας περιλαμβάνει 3 κύριες ομάδες: μέταλλα, μεταλλοειδή και μη μέταλλα. Για παράδειγμα, τα στοιχεία που βρίσκονται στο κάτω και αριστερό άκρο του πίνακα είναι τα πιο μεταλλικά και τα στοιχεία που βρίσκονται πάνω δεξιά είναι τα λιγότερο μεταλλικά. (π.χ. το καίσιο είναι πολύ πιο μεταλλικό από το ήλιο). Υπάρχουν επίσης πολλά άλλα μοτίβα και σχέσεις.
Ο περιοδικός πίνακας επινοήθηκε από τον Ρώσο χημικό Ντμίτρι Ιβάνοβιτς Μεντελέγιεφ (1834-1907). Προς τιμήν του, το στοιχείο 101 πήρε το όνομά του, mendelevium.
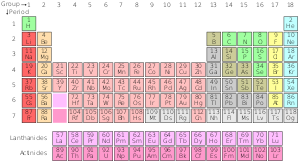
Η τυπική παραλλαγή του περιοδικού πίνακα
Τυποποιημένος περιοδικός πίνακας
| Ομάδα → | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 12 | 13 | 14 | 15 | 16 | 17 | ||||
| 1 | 2 | |||||||||||||||||||
| 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||||||||||||
| 3 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||
| 4 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 | 36 | ||
| 5 | 37 | 38 | 39 | 40 | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 50 | 51 | 52 | 53 | 54 | ||
| 6 | 55 | 56 | * Λανθανίδες | 72 | 73 | 74 | 75 | 76 | 77 | 78 | 79 | 80 | 81 | 82 | 83 | 84 | 85 | 86 | ||
| 7 | 87 Fr | 88 | ** Ακτινίδια | 104 | 105 | 106 | 107 | 108 | 109 | 110 | 111 | 112 | 113 | 114 | 115 | 116 | 117 | 118 | ||
| 8 | 119 Uue | 120 Ubn | *** Υπερακτινίδια | |||||||||||||||||
| * Σειρά λανθανιδίων | 57 | 58 | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | 69 | 70 | 71 | |||||
| ** Σειρά ακτινιδίων | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 | |||||
| *** Σειρά υπερακτινιδίων | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129Ube | 130Utn | 131Utu | 132Utb | 133Utt | 134Utq | 135Utp | |||||
| *** Σειρά υπερακτινιδίων | 136η | 137Uts | 138Uto | 139Ute | 140Uqn | 141Uqu | 142Uqb | 143Uqt | 144Uqq | 145Uqp | 146Uqh | 147Uqs | 148Uqo | 149Uqe | 150Upn | |||||
| *** Σειρά υπερακτινιδίων | 151Upu | 152Upb | 153Upt | 154Upq | 155Upp | 156Uph | 157Ups | 158Upo | 159Upe | 160Uhn | 161Uhu | 162Uhb | 163Uht | 164Uhq | 165Uhp | |||||
| *** Σειρά υπερακτινιδίων | 166Uhh | 167Uhs | 168Uho | 169Uhe | 170Usn | 171Usu | 172Usb | 173Ust | 174Usq | 175Usp | 176Ush | 177Uss | 178Uso | 179Χρήση | 180Uon | |||||
| *** Σειρά υπερακτινιδίων | 181Uou | 182Uob | 183Uot | 184Uoq | 185Uop | 186Uoh | 187Uos | 188Uoo | 189Uoe | 190Uen | 191Ueu | 192Ueb | 193Uet | 194Ueq | 195Uep | |||||
| *** Σειρά υπερακτινιδίων | 196Ueh | 197Ues | 198Ueo | 199Uee | 200Bnn | 201Bnu | 202Bnb | 203Bnt | 204Bnq | 205Bnp | 206Bnh | 207Bns | 208Bno | 209Bne | 210Bun | |||||
| *** Σειρά υπερακτινιδίων | 211Buu | 212Bub | 213Αλλά | 214Buq | 215Bup | 216Buh | 217Bus | 218Buo | 219Bue | 220 δισ. | 221Bbu | 222Bbb | 223Bbt | 224Bbq | 225Bbp | |||||
Χημικές σειρές του Περιοδικού Πίνακα
- Αλκαλικά μέταλλα
- Αλκαλικές γαίες
- Λανθανίδες
- Ακτινίδια
- Υπερακτινίδια
- Μέταλλα μετάπτωσης
- Φτωχά μέταλλα
- Μη μέταλλα
- Αλογόνα
Κατάσταση σε κανονική θερμοκρασία και πίεση. Το χρώμα του αριθμού (ατομικός αριθμός) πάνω από το σύμβολο του στοιχείου δείχνει την κατάσταση του στοιχείου σε κανονικές συνθήκες.
- τα αέρια με μπλε χρώμα
- τα πράσινα είναι υγρά
- τα μαύρα είναι συμπαγή
- Εκείνα με συμπαγή όρια έχουν σταθερά ισότοπα (αρχέγονα στοιχεία)
- Εκείνα με διακεκομμένα όρια έχουν μόνο ραδιενεργά φυσικά ισότοπα.
- Εκείνα με διακεκομμένα όρια δεν απαντώνται στη φύση (συνθετικά στοιχεία)
- όσοι δεν έχουν σύνορα είναι πολύ ραδιενεργοί για να έχουν ανακαλυφθεί ακόμη.
Άλλες μέθοδοι απεικόνισης των χημικών στοιχείων
Η έκδοση του περιοδικού πίνακα που παρουσιάζεται παραπάνω είναι αυτή που χρησιμοποιείται περισσότερο. Άλλες ευρέως διαδεδομένες εκδόσεις παρουσιάζονται παρακάτω:
· 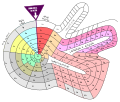
Ο Theodor Benfey τοποθέτησε τα στοιχεία σε μια σπείρα, γύρω από το υδρογόνο. Το ατομικό βάρος καθορίζει τη θέση του στοιχείου.
· 
Ο Ντμίτρι Ιβάνοβιτς Μεντελέγιεφ χρησιμοποίησε μια διάταξη λουλουδιών- τα ακτινίδια, τα λανθανίδια εμφανίζονται ως βρόχοι δίπλα στην κύρια ομάδα.
· 
Ο Timothy Stove ταξινόμησε τα στοιχεία με βάση τον κβαντικό αριθμό.
· ![]()
Ο Betterman ταξινόμησε τα στοιχεία με βάση τις ισοηλεκτρικές τους ιδιότητες, οι οποίες μπορούν να μετατραπούν σε πολυωνυμική μορφή.
· 
Τριγωνική έκδοση, από τους Zmaczynski και Bayley
· 
Τοποθετημένα σε πυραμίδα.
Εκδόσεις που χρησιμοποιούνται λιγότερο
- Ο τυποποιημένος πίνακας παρέχει τα βασικά. Φαίνεται παραπάνω
- Ένας κάθετος πίνακας για βελτιωμένη αναγνωσιμότητα στα προγράμματα περιήγησης ιστού
- Ο μεγάλος πίνακας παρέχει τα βασικά καθώς και τα πλήρη ονόματα των στοιχείων
- Ο τεράστιος πίνακας παρέχει τα βασικά στοιχεία καθώς και τα πλήρη ονόματα των στοιχείων και τις ατομικές μάζες.
- Διαμορφώσεις ηλεκτρονίων
- Μέταλλα και μη μέταλλα
- Κατάλογος στοιχείων: περιλαμβάνει όνομα, σύμβολο, ατομικό αριθμό, ατομική μάζα, ομάδα και περίοδο- δυνατότητα ταξινόμησης με βάση οποιοδήποτε από αυτά.
- Κατάλογος στοιχείων ανά σύμβολο
- Κατάλογος στοιχείων με βάση το σημείο βρασμού
- Κατάλογος στοιχείων με βάση το σημείο τήξης
- Κατάλογος στοιχείων με βάση την πυκνότητα
Σχετικές σελίδες
- Ομάδα περιοδικού πίνακα
- Περίοδος περιοδικού πίνακα
- Διευρυμένος περιοδικός πίνακας
Ερωτήσεις και απαντήσεις
Q: Τι είναι ο περιοδικός πίνακας;
A: Ο περιοδικός πίνακας είναι ένας πίνακας που ταξινομεί όλα τα γνωστά χημικά στοιχεία κατά σειρά των ατομικών τους αριθμών, ξεκινώντας με το υδρογόνο στο νούμερο ένα. Στοιχεία με παρόμοια χαρακτηριστικά τοποθετούνται συχνά το ένα κοντά στο άλλο.
Ερ: Πόσες περίοδοι και ομάδες υπάρχουν στον τυπικό περιοδικό πίνακα;
Α: Στον τυποποιημένο περιοδικό πίνακα υπάρχουν 8 περίοδοι και 18 ομάδες.
Ερ: Τι κοινό έχουν τα στοιχεία μιας περιόδου;
Α: Τα στοιχεία μιας περιόδου έχουν διαδοχικούς ατομικούς αριθμούς.
Ερ: Τι κοινό έχουν τα στοιχεία μιας ομάδας;
Α: Τα στοιχεία μιας ομάδας έχουν ηλεκτρόνια τοποθετημένα με παρόμοιο τρόπο, ανάλογα με τον αριθμό των ηλεκτρονίων σθένους, γεγονός που τους προσδίδει παρόμοιες χημικές ιδιότητες.
Ερ: Ποιος εφηύρε τον περιοδικό πίνακα;
Α: Ο Ρώσος χημικός Ντμίτρι Ιβάνοβιτς Μεντελέγιεφ (1834-1907) εφηύρε τον περιοδικό πίνακα.
Ερ: Ποιες είναι οι τρεις κύριες ομάδες του περιοδικού πίνακα;
Α: Οι τρεις κύριες ομάδες του Περιοδικού Πίνακα είναι τα μέταλλα, τα μεταλλοειδή και τα μη μέταλλα.
Ερ: Πώς μπορούν να παρατηρηθούν μοτίβα και σχέσεις μεταξύ των στοιχείων χρησιμοποιώντας τον Περιοδικό Πίνακα;
Α: Μοτίβα και σχέσεις μεταξύ των στοιχείων μπορούν να παρατηρηθούν κοιτάζοντας πού εμφανίζονται στον Περιοδικό Πίνακα- για παράδειγμα, τα στοιχεία που βρίσκονται κάτω αριστερά του τείνουν να είναι πιο μεταλλικά από εκείνα που βρίσκονται πάνω δεξιά.
ψάχνω